올해의 노벨 생리의학상 수상 영예는 산소 농도의 변화에 어떻게 생명체가 세포차원에서 적응했는지를 밝힌 3명의 영국, 미국 연구자들에게 돌아갔다. 미국의 윌리엄 케일린과 그레그 서멘자, 영국의 피터 랫클리프다. 이들의 연구결과는 암과 빈혈을 비롯한 다양한 질병들을 극복할 수 있는 유망한 전략을 제시한 것으로 평가 받는다.
스웨덴 카롤린스카 연구소 노벨위원회는 7일(현지시간) 이들 3명을 노벨 생리의학상 공동수상자로 선정했다고 밝혔다. 산소 농도에 따른 세포의 적응 기전에 관한 연구 공로를 인정한 결과다. 이들 수상자는 다양한 산소 농도에 반응해 유전자의 활동을 조절하는 일종의 ‘세포 공장’들을 밝혀냈다고 위원회는 설명했다. 특히 세포가 산소의 저농도에 적응하는 과정에 ‘HIF-1’라는 명칭의 유전자가 중요한 역할을 하는 것을 밝힌 것이 수상자들 공로의 요체다.
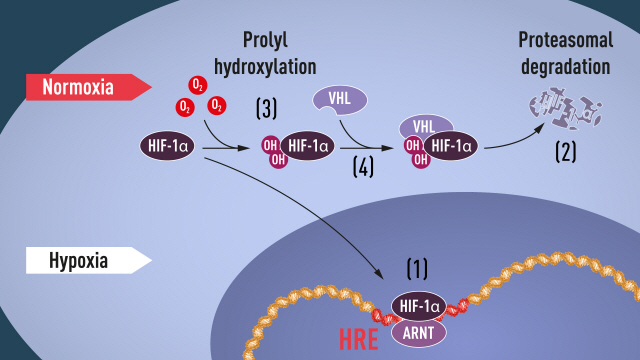
지구 생명의 진화과정에서 세포와 조직에 충분히 산소를 공급하기 위한 메커니즘이 발전해왔다. 특히 산소농도가 떨어져 저산소증이 발생하면 인체에선 적혈구 생성을 촉진하는 에리스로포이에틴 호르몬(EPO)이 증가해 적혈구 세포의 생성 증가를 유도한다. 서멘자는 이 같은 반응을 유전자 차원에서 조절하는 단백질 복합체인 저산소-유동성 인자(HIF)를 발견했다. HIF의 단백질 중에서도 ‘HIF-1α’는 세포내 산소농도가 낮아지면 증가하고, 산소 농도가 높아져 정상화되면 분해돼 양이 줄어든다. 랫클리프와 케일린은 하이드록실기의 일종인 ‘프로릴 수산화효소’가 HIF-1α에 붙어 분해되도록 유도한다는 것을 밝혀냈다.
위원회는 이들 3명의 연구가 미친 영향에 대해 “학계 실험실 및 제약회사가 지속적인 노력으로 산소 감지 시스템을 활성, 또는 차단해서 다른 질병 상태를 개선할 수 있는 약물 개발에 나섰다”고 평가했다. /민병권·우영탁기자 newsroom@sedaily.com