올해의 노벨 생리의학상 수상 영예는 산소 농도의 변화에 어떻게 생명체가 세포차원에서 적응했는지를 밝힌 3명의 영국, 미국 연구자들에게 돌아갔다. 미국의 윌리엄 케일린과 그레그 서멘자, 영국의 피터 랫클리프가 그 주인공이다. 이에 따라 이들의 연구를 바탕으로 한 신약 개발 현황에도 관심이 쏠리고 있다. 케일린은 취재진과의 전화통화에서 “나를 비롯해 수상자들은 산소 적응과 관련 저산소유도인자(HIF) 단백질 조절을 새로운 치료 실마리로 제시한 것”이라며, 그러한 신약 후보물질이 개발단계에 있다고 소개했다.
12일 제약, 바이오 업계에 따르면 아스트라제네카와 파브로젠, 아스텔라스가 함께 개발 중인 빈혈약 ‘록사두스타트’가 HIF 단백질을 활용한 신약 중 가장 앞선 것으로 평가된다. 중국, 일본 등에서 이미 시판허가를 받았고 연내 미국 식품의약국(FDA)에 품목허가를 신청할 예정이다. 이 약은 빈혈 환자에게 적혈구를 생성하는데, 신장투석환자에게 인기가 많다. 그동안 신장투석환자가 적혈구를 생성하기 위해서는 주기적으로 주사를 맞아야 했는데, 이를 먹는 약으로 바꿨기 때문이다.
국내 바이오기업들도 HIF를 활용한 치료제 개발에 나섰다. 크리스탈지노믹스는 HIF를 활용한 염증성 장질환 치료제 ‘CG-598’을 개발하고 있다. 이 치료제는 HIF를 안정화해 손상된 세포장벽을 복구한다. 대장에 염증이 생기는 염증성장질환은 아직까지 원인이 밝혀지지 않아 치료가 쉽지 않다. 크리스탈지노믹스는 쥐를 대상으로 한 동물실험에서 염증성장질환을 인위적으로 발생시킨 두 모델 모두에서 치료효과를 확인했다고 밝혔다.
RNA 치료제를 개발 중인 올리패스 역시 HIF 단백질을 표적으로 한 비소세포폐암 치료제를 개발하고 있다. 현재 전임상 중이지만 2022년까지 기술이전을 성사하겠다는 목표로 개발 중에 있다.
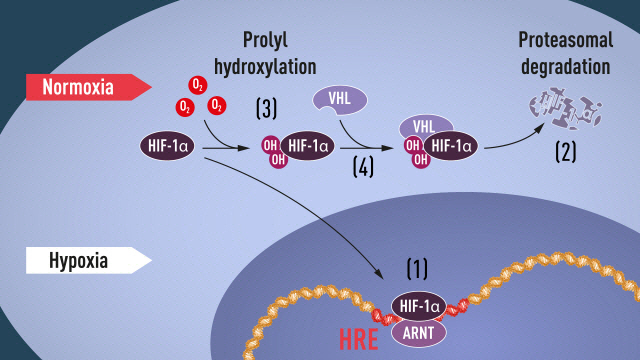
한편 노벨 생리의학상 수상자인 서멘자는 산소농도가 떨어져 저산소증이 발생하면 인체에선 적혈구 생성을 촉진하는 에리스로포이에틴 호르몬(EPO)이 증가해 적혈구 세포의 생성 증가를 유도하는 반응에서 유전자 차원에서 조절하는 단백질 복합체인 저산소-유동성 인자(HIF)를 발견했다. HIF의 단백질 중에서도 ‘HIF-1α’는 세포내 산소농도가 낮아지면 증가하고, 산소 농도가 높아져 정상화되면 분해돼 양이 줄어든다. 랫클리프와 케일린은 하이드록실기의 일종인 ‘프로릴 수산화효소’가 HIF-1α에 붙어 분해되도록 유도한다는 것을 밝혀냈다.