영국·남아공·브라질발(發) 코로나19 바이러스 변이체들이 전 세계를 긴장시키고 있다. 해외 입국자를 중심으로 국내에서도 감염자가 나와 지구촌 시대를 실감케 한다.
영국·독일 등 유럽을 포함한 많은 국가들이 학교·상점 등의 문을 닫는 봉쇄 조치에 들어가거나 해외 입국자, 특히 영국·남아공·브라질발 입국자에 대한 방역 강화에 나서게 만든 이런 변이체들은 이전의 바이러스와 어떤 공통점과 차이점을 갖고 있을까.
유전자 염기서열 차이로 인한 아미노산의 변화를 기준으로 남아공발 변이 바이러스는 국내에서 가장 많은 감염자가 나온 GH 계통군(clade), 영국·브라질발 변이 바이러스는 GR 계통군으로 분류된다.
◇스파이크 D614G·N501Y 변이 공통적
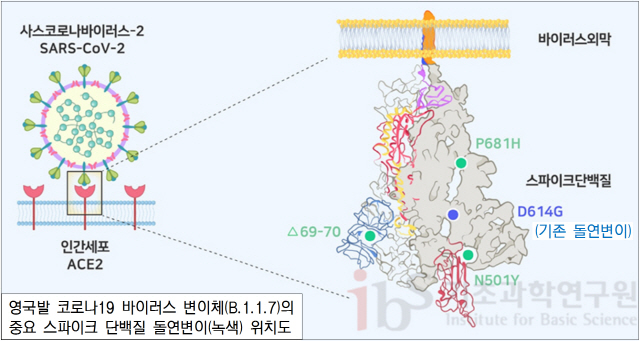
두 계통군 모두 코로나19 바이러스가 사람을 감염시킬 때 관문·교두보 역할을 하는 사람 세포의 앤지오텐신전환효소2(ACE2) 수용체에 달라붙는 스파이크 단백질의 1,273개 아미노산 가운데 614번째가 아스파틱산(D)에서 글리신(G)으로 바뀌어 있다. D614가 G614로 바뀐 D614G 변이다. 스파이크에 G614가 포함된 변이 바이러스는 ACE2 수용체에 더 단단히 달라붙어 감염률과 감염속도를 높임으로써 지난해 중·하반기 코로나19의 대유행에 상당한 역할을 했다.
지난해말부터 주목을 받고 있는 영국·남아공·브라질발 변이체들은 D614G 변이 외에도 비슷한 기능을 하는 N501Y 변이 등이 추가돼 감염률과 감염속도를 가속화하고 있다.
N501Y 변이는 사람 ACE2 수용체와 결합하는 스파이크의 맨 끝 부위에서 발생한다. 스파이크 단백질의 501번째 아미노산 위치에서 아스파라긴(N)이 티로신(Y)으로 바뀌어 사람 ACE2 수용체에 대한 친화성을 증가시켜 더 단단히 결합할 수 있게 해준다.
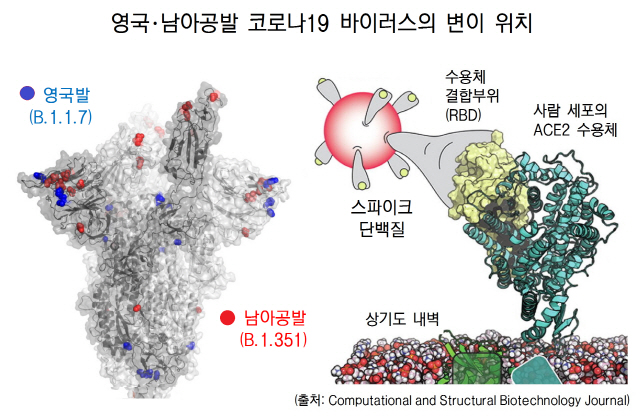
이런 공통점 때문에 영국·남아공·브라질발 변이 바이러스는 각각 501Y.V1와 V2, V3라는 약칭으로 불린다. V는 변이체(variant)를 뜻한다. 다양한 변이를 포괄하는 계통(Lineage) 분류체계에 따라 B.1.1.7, B.1.351, B.1.1.28.1(또는 P.1)로 분류하기도 한다.
◇영국발 B.1.1.7, 게놈 서열 등록 1만8,070건
3개 변이체 가운데 세계 각국에 가장 널리 퍼진 것은 영국발 B.1.1.7(501Y.V1). 영국에서 지배적인 코로나19 변이체가 된데 이어 총 40개국에서 1만8,070건(18일 오후 7시 기준)의 B.1.1.7 변이체 게놈 서열을 GISAID(Global Initiative on Sharing All influenza Data)에 등록했다. 감염자가 많고 게놈 분석도 활발한 영국(1만6,982건), 덴마크(192건), 네덜란드(95건), 이스라엘(89건), 미국(86건) 순이며 한국도 3건의 게놈 서열을 등록했다. 실제 B.1.1.7 감염자는 나라에 따라 게놈 분석 비율이 천차만별이며 몇배~수십배에 이를 것으로 보인다.
B.1.1.7은 17개의 아미노산 변이 중 8개가 스파이크 단백질에서 발견된다. 특히 69·70번째 아미노산이 없는 이중결실(69-70del), 이 단백질이 잘리는 부위 바로 옆에서 발생한 P681H 변이는 스파이크의 모양·구조 등에 영향을 미쳐 감염률·세포침투력을 높이는 것으로 추정된다. 최근 기도 상피세포에 ACE2 수용체가 많지 않은 어린이에서 감염자가 늘고 있는데 B.1.1.7의 이런 변이가 영향을 미친 것으로 전문가들은 보고 있다. 물론 성인의 상부 호흡기에 바이러스가 더 높은 농도로 증식해 증상이 더 심해질 수도 있다.
앞서 유럽질병통제예방센터(ECDC)는 “(B.1.1.7이) 기존 전파 속도보다 최대 70% 빨라 감염재생산지수를 1.1에서 1.5로 늘렸다”고 발표했다. 미국 질병통제예방센터(CDC) 연구진도 B.1.1.7이 오는 3월이면 미국에서 우세한 변이체 계통으로 자리잡을 가능성이 크다고 전망했다.
남아공발 B.1.351(501Y.V2)과 P.1 계통이라고도 불리는 브라질발 B.1.1.28.1(501Y.V3)은 D614G, N501Y와 함께 E484K라는 스파이크 단백질 아미노산이 변이된 공통분모를 갖고 있다. E484K 변이는 코로나19 완치자의 회복기 혈청 및 단일클론 항체와 반응시킨 실험에서 항체의 중화 효능이 감소하는 것으로 나타나 우려를 키우고 있다. 스파이크 단백질 부위에 이런 변이들이 누적돼 스파이크의 모양·구조가 달라질수록 백신 접종으로 유도된 사람의 항체나 직접 투여한 항체(항체치료제)가 스파이크 단백질에 단단하게 달라붙지 못해 바이러스가 사람 세포로 침투하는 것을 막는 중화 효능이 떨어진다. 백신·항체치료제 ‘설계’ 변경으로 대응하면 되지만 임상시험 등 복잡한 과정을 동반해야 할 수 있다.
이와 관련 국립보건연구원의 김은진 신종병원체분석과장은 “변이 사이트 하나하나에 대한 실험실 연구결과와 다양한 변이 사이트를 가진 바이러스의 전파력 및 인체의 항체·면역반응에 실제로 미치는 영향 간에는 차이가 있을 수 있다”며 과도한 공포감을 경계했다.
실제로 화이자와 모더나는 미국·유럽 등에서 긴급사용승인된 자사의 mRNA 코로나19 백신이 “변이 바이러스에 대해서도 똑같이 반응했다”는 실험실 연구결과를 발표했다.
안광석 서울대 생명과학부 교수(기초과학연구원 RNA연구단 연구위원)는 “지난해 7월 미국 연구진이 (가상 바이러스와 배양세포 수준의 실험실 조건에서 얻은 결과를 바탕으로) D614G 변이가 바이러스의 전파력을 6배까지 증가시킬 수 있다는 연구결과를 발표했지만 후속 연구에선 전파력이 약간 증가한 것으로 나타났다”며 “B.1.1.7의 유행도 변이체 고유의 전파력에서 기인한 것인지, (계절적 요인과) 영국의 특수한 코로나19 대응방식·사회적 요인이 반영된 결과인지 상관관계가 아직 명확하지 않다”고 말했다.