우후죽순 쏟아졌던 복제약(제네릭)의 출시가 잦아들었다. ‘아토젯’과 같은 대형 오리지널 의약품의 특허 만료로 인한 제네릭 허가 폭증이 4월에 정점을 찍은 뒤 한 풀 꺾인데다 지난해 7월부터 시행된 계단식 약가제도도 일부 영향을 미친 결과로 풀이된다. 업계는 국회가 입법 추진 중인 ‘공동생동 1+3 제한법’이 제네릭 시장에 미칠 여파에도 촉각을 곤두 세우고 있다.
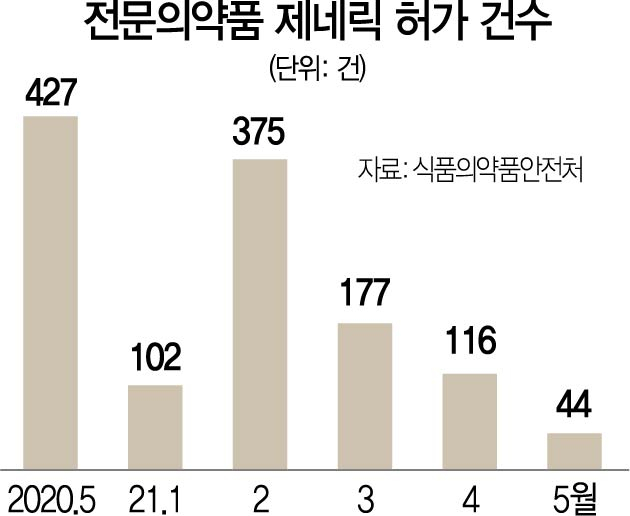
23일 식품의약품안전처에 따르면 지난 5월 전문약 제네릭 허가 건수는 총 44건이다. 지난해 같은 기간(427건) 대비 약 10분의1 수준으로 급감했다. 직전 달인 4월(116건)과 비교해봐도 62.1%가 줄었다. 지난해 10월(43건) 이후 7개월 래 가장 낮은 허가 건수다.
가장 큰 원인은 대형 오리지널 의약품인 고지혈증 복합제 아토젯 관련 제네릭 허가가 지난 4월 마무리 됐기 때문이다. 또 다른 배경은 계단식 약가제다. 계단식 약가제는 등재 순서대로 20품목까지는 자체 생동 시험과 원료 의약품 사용 등 2가지 기준 요건 모두 총족 시 오리지널 의약품 대비 53.55%, 1개 미충족시 45.52%, 2개 미충족시 38.69%를 각각 상한가로 정하도록 한 제도다. 21품목부터는 기존 최저가의 85%에서 가격이 책정된다.
동일한 생물학적동등성시험 자료를 활용해 허가를 받을 수 있는 품목 수를 최대 4개로 제한하는 약사법 개정안도 앞으로 제네릭 시장에 영향을 끼칠 것으로 보인다. 현재는 허가 받을 수 있는 품목 수에 제한이 없다보니 제네릭이 과하게 양산되고 있다. 1+3 제한법은 지난 16일 국회 보건복지위원회 전체회의를 통과했다. 여야 의원 간 이견이 없어 조만간 법제사법위원회 전체회의와 국회 본회의를 통과할 것으로 보인다. 업계 한 관계자는 “공동 생동 1+3 제한법이 통과되면 과열된 시장이 다소 식을 것”이라면서도 “하지만 1~20위 내에 들기 위한 경쟁은 여전히 거셀 것"이라고 전했다. 이 관계자는 다만 "다른 대형 오리지널 의약품 특허가 만료되면 제네릭 시장이 다시 과열될 가능성은 여전히 열려 있다”고 덧붙였다.
/임지훈 기자 jhlim@sedaily.com