|
셀트리온이 식품의약품안전청(KFDA)으로부터 바이오시밀러의 제품 허가를 받았다는 소식에 사흘 연속 강세를 보였다.
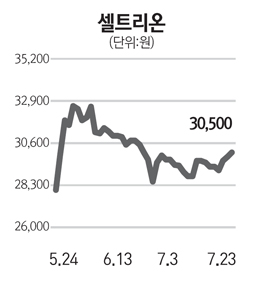
23일 코스닥시장에서 셀트리온은 장 중 내내 강세를 보인 끝에 0.99%(300원) 오른 3만500원으로 장을 마감했다. 이로써 셀트리온은 사흘간 4.10% 올랐다.
셀트리온이 최근 강세를 보인 것은 자가면역질환 항체 치료제인 ‘램시마(Remsima)’가 식약청으로부터 제품 허가를 받았기 때문으로 풀이된다. 식약청이 글로벌 임상결과를 근거로 바이오시밀러에 대한 제품 허가를 낸 것은 이번이 처음. ‘램시마’는 류마티스 관절염과 강직성 척추염, 궤양성 대장염, 크론병, 건선 등 적응증에 대한 제품 허가를 받았다. 셀트리온은 약가 등재 과정 등을 거쳐 이르면 오는 3ㆍ4분기 내 셀트리온제약을 통해 국내에 제품을 출시할 계획이다. 셀트리온은 지난 2006년 물질 개발을 시작으로 7년간 2,000억원을 글로벌 임상 등에 투자한 바 있다.
셀트리온 측 관계자는 “식약청 제품 허가로 램시마는 28조원 규모의 TNF-알파 억제 항체 치료제 시장을 공략할 기반을 마련하게 됐다”며 “지난 3월 유럽의약청(EMA)에 낸 제품 허가신청도 이르면 내년 상반기 중 통과될 가능성이 커 앞으로 램시마 매출이 본격화될 수 있다”고 설명했다.
이 관계자는 이어 “이 밖에 다른 바이오시밀러에 대한 상용화 준비도 진행 중”이라며 “‘허셉틴’바이오시밀러 등에 대한 국내외 제품 허가도 내년부터 진행할 것”이라고 덧붙였다. 셀트리온은 허셉틴 바이오시밀러의 경우 내년 하반기 국내와 유럽 등지에 제품 허가를 추진할 계획이다. 또 브라질과 스페인, 그리스, 러시아 증지에서 리톡산 바이오시밀러에 대한 임상 1상과 3상을 진행하고 있다.