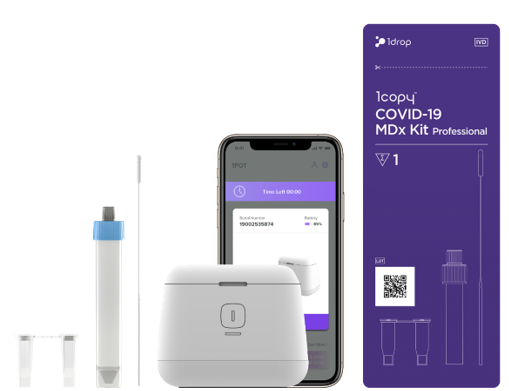
이번에 승인된 (주)원드롭의 신제품은 국내 최초 분자진단 기술 기반의 현장형 코로나19 진단 솔루션이다.
이 제품은 기존 면역진단검사의 편리성과 qPCR 진단 수준의 정확도를 가지며, 사용자는 검체 채취 후 별도의 유전자 추출과정 없이 최소 22분이내에 간단히 스마트폰 앱을 통해 결과를 편리하고 정확하게 확인 및 관리할 수 있다. 이와 더불어 시약의 실온 보관 및 배송이 가능한 것이 특징이며, 기존 분자진단 검사 대비 합리적인 가격으로 공급될 예정이다.
임상적 성능시험기관의 3자 비교 시험 결과, 표준진단법인 qPCR 진단키트의 일반적인 측정영역인 Ct값 35이내의 검체에서 민감도, 특이도가 각각 100%인 것으로 확인되었으며, 이는 qPCR진단법과 유사한 성능으로 볼 수 있다.
(주)원드롭은 이번 식약처 수출허가를 계기로 헝가리, 우크라이나, 미국, 남아프리카공화국 등 해외 판매 국가를 확대해 나갈 것이며, 분자진단 검사소를 구축하기 어려운 동남아 국가에 우선적으로 이동형 검사 사업을 추진할 계획이다.
(주)원드롭 이주원 대표는 “현재 시장 확대를 위해 FDA-EUA 등 각국 판매허가 및 국내/외 전문가/개인용 인허가 획득을 추진 중으로 보건소 및 보건지소, 앰뷸런스, 응급실 등에 공급하여 국내 사업을 시작할 예정이다”라고 밝혔다.
그는 이어 “분자진단 수준의 정확도와 면역진단 수준의 편리성을 가진 제품에 대한 시장의 요구에 부응하기 위해 노력한 결과 이번 신제품을 출시하게 되었다.
코로나19감염증은 팬데믹을 넘어 앤데믹(풍토병화)화 될 것으로 판단되며 당사의 1copy™ COVID-19 MDx Kit Professional 제품은 향후 국내외 코로나19감염증 관리에 있어 최적의 진단 솔루션으로 활용될 것으로 기대한다.
또한, 이번 신제품을 플랫폼화 하여 코로나19감염증을 시작으로 독감, 성병, 간염, 말라리아 등 컨텐츠를 지속적으로 확장하고 기존 당사 제품군인 당뇨, 통풍, 빈혈, 고지혈증 등 만성질환 관리 솔루션과 통합한 토탈 시스템을 구축하여 혁신적인 모바일 헬스케어 서비스를 제공할 예정이다.”라고 밝혔다.
한편, 2017년 설립된 (주)원드롭은 삼성전자 C-Lab 스핀오프 기업으로 상용 스마트폰 기반의 만성질환 관리 솔루션과 단일분자까지 정량 가능한 분자진단 기술을 바탕으로 분자진단키트를 연구 개발, 제조 및 판매하고 있다. 최근 핵산 비추출 방식(extraction-free) PCR 기술 개발, 코로나19/독감/RSV 동시진단 키트를 출시하였고, FDA-EUA 및 19개국 이상의 판매허가를 획득한 후 50여개국에 총200만 테스트 이상의 진단키트를 공급하고 있다.