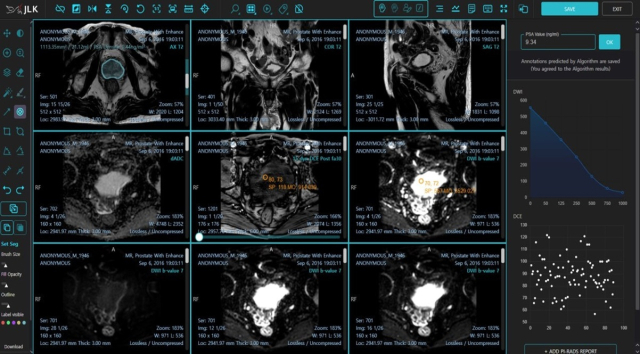
제이엘케이(322510)는 미국 식품의약국(FDA)에서 전립선암 진단 인공지능(AI) 솔루션의 510(k) 승인을 획득했다고 24일 밝혔다.
FDA 승인을 받은 제이엘케이 제품은 전립선암 진단 AI 솔루션인 ‘메디허브 프로스테이트(MEDIHUB Prostate)’다. 제이엘케이가 서울아산병원, 미국 미주리 대학과의 임상시험으로 개발했다.
제이엘케이에 따르면 전립선암 진단과 추적에는 다중 매개변수 전립선 자기공명영상(MRI)이 활용된다. 하지만 질병에 대한 조직학적 이해와 MRI 영상 경험이 요구되는 등 전립선암 진단에는 난이도가 있다. 전 세계적으로 인증된 바이오마커(생체 지표) PIRADS(Prostate Imaging Reporting and Data System) 점수가 사용된다.
제이엘케이의 메디허브 프로스테이트는 AI를 활용해 다중 매개변수 전립선 MRI를 복합적으로 분석하고 PIRADS 진단 및 전립선특이항원(PSA) 밀도 진단 등 전립선암 진단에 필요한 모든 데이터를 제공해준다. 특히 전립선암 진단 시장의 성장성이 높다는 점은 제이엘케이에 유리한 요인다. 국제암연구소에 따르면 전립선암은 경제협력개발기구(OECD) 남성에게 가장 발병하기 쉬운 암 중 하나다. 미국 남성에게 가장 흔한 암 1위이기도 하다. 제이엘케이에 따르면 미국에서는 매년 28만 8300건 이상의 전립선암 신규 진단이 나온다.
김동민 제이엘케이 대표는 “올해 5개 솔루션을 FDA에 신청하고 그 중 최소 1개 솔루션에 대해서는 미국의 보험 수가까지 획득한다는 목표를 세웠다”며 “첫 FDA 승인을 기반으로 미국 진출 계획을 더 공격적으로 수정하는 등 승부를 걸 수 있도록 진입 전략을 재수립할 것”이라고 말했다.