전 세계가 신종 코로나바이러스 감염증(코로나19)에 몸살을 앓고 있다. 백신이나 치료제가 개발될 때까지 코로나19 유행이 이어질 것이라는 암울한 전망도 제기되고 있다. 이에 전세계 제약바이오기업들이 코로나19 치료제와 백신 개발에 뛰어들었다. 국내에서도 다수의 바이오벤처가 코로나19 백신과 치료제 개발에 나섰다고 밝혔지만 업계에서는 주가 부양을 위해 실현 가능성이나 기대 수익이 적은데도 무작정 정제되지 않은 정보를 흘리고 있다고 보고 있다. 무리한 주가부양으로 시장의 신뢰를 깎는 제2의 ‘인보사 사태’가 재발할 수 있다는 목소리도 나온다.
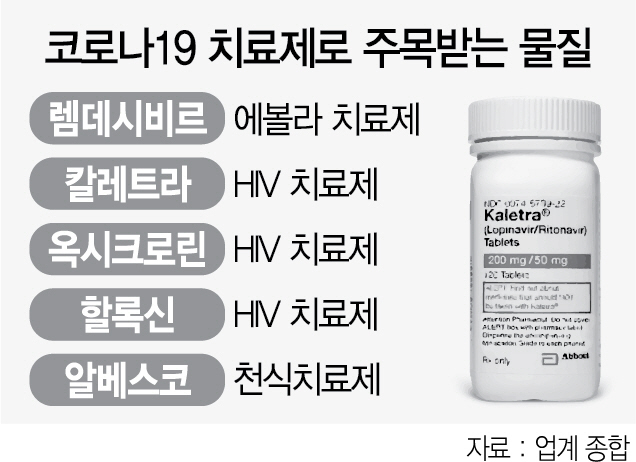
30일 제약바이오업계에 따르면 국내 제약바이오기업 가운데 10개 이상의 업체가 치료제 개발에 나섰으며 백신 개발에도 5개 이상 업체가 뛰어들었다. 하지만 이 중 식품의약품안전처의 임상시험 허가를 얻어낸 회사는 없다. 식약처에 따르면 이날 기준 임상시험 계획이 승인된 치료제는 길리어드의 에볼라 치료제 ‘렘데시비르’, 인간면역결핍바이러스(HIV) 치료제 ‘칼레트라’·‘옥시크로린’·‘할록신’, 천식치료제 ‘알베스코’ 뿐이다. 이 중 즉시 상업화가 가능한 허가용 임상은 ‘렘데시비르’의 임상 3상 뿐이다. 나머지 치료제는 병원의 연구용으로 진행하는 ‘연구자 임상시험’이다.
코로나바이러스는 단일 가닥의 RNA바이러스다. 복제도 빠르고 변이도 다양하게 일어난다. 코로나바이러스 중 사람에게 질병을 유발하는 바이러스는 7종인데 7종 모두 치료제와 백신이 없다. 메르스·사스·코로나19를 제외한 4종은 가벼운 감기를 일으킬 뿐이라 치료제의 필요성이 낮았고 메르스와 사스는 치명률이 높았지만 막대한 돈을 들여 치료제를 개발하기에는 너무 적은 사람만 걸렸다.
이 때문에 섣불리 코로나19 치료제나 백신 개발에 뛰어들기 어렵다. 개발 자체에만 최소 4~5년이 걸리는데, 개발 도중 글로벌 제약사가 먼저 치료제를 개발하고 시장을 선점할 가능성이 높은데다, 인플루엔자보다 시장 규모도 훨씬 작기 때문이다. 2009년 유행했던 신종플루는 국내에서만 70만명이 감염됐다. 한 바이오업체 대표는 “국내에서 코로나19 치료제나 백신을 개발하더라도 투입한 개발비만큼의 수익을 거두기란 쉽지 않을 것”이라며 “주가 부양 목적이 아니라 실제로 코로나19 치료제나 백신을 개발하는 회사라면 절대 투자하면 안 되는 회사”라고 밝혔다.
이승규 한국바이오협회 부회장 역시 “진단업체의 경우 국내의 코로나19 대규모 유행 시점이 해외보다 빨랐고 그 와중에 역량을 쌓을 수 있어 지금의 실적이 나오는 것”이라며 “진단키트와 치료제 개발은 걸리는 시간 자체가 다른 만큼 주의해야 한다”고 강조했다. 그는 이어 “잘못된 주가 부양으로 국내 바이오기업의 신뢰가 또 무너지는 것은 아닌가 걱정된다”고 덧붙였다.