세계 최대 암 관련 학술대회인 미국 임상종양학회(ASCO) 2022년 연례회의가 일리노이주 시카고에서 7일(현지시간) 폐막한 가운데 한국 바이오 벤처 기업들이 의미있는 성과를 냈다. 3년 만에 대면으로 열린 이번 회의에서 신약 후보물질 임상 시험 결과를 대거 발표했고, 글로벌 대형 제약사를 대상으로 한 기술수출의 자신감을 나타냈다. ASCO 연례회의는 학술 행사일뿐만 아니라 사업기회 발굴과 투자유치의 장이기도 하다.
7일 업계에 따르면 HLB(028300)는 이번 ASCO 2022에서 함암 신약 ‘리보세라닙’의 선양낭성암 임상 2상 결과를 발표해 주목을 받았다. 임상을 주도한 강현석 미 캘리포니아대 샌프란시스코 의대 교수는 “6개월 이내 급격히 악화된 환자들을 대상으로 리보세라닙을 투여한 결과 80% 이상의 환자에게서 암 성장 억제 효과가 있는 것을 확인했다”며 “아직까지 미 식품의약국(FDA) 허가를 받은 약물이 없는 선낭암 분야에서 리보세라닙이 세계 최초의 1차 치료제로 개발될 가능성이 높다”고 강조했다. HLB는 미 FDA와 가속승인 및 신약승인신청(NDA)을 위한 논의를 조속히 시작할 방침이다. 아울러 이번 임상 시험에 참여한 링빙 멍 미 모핏 암연구센터 연구원은 ASCO 2022 주최측으로부터 공로상을 받기도 했다.
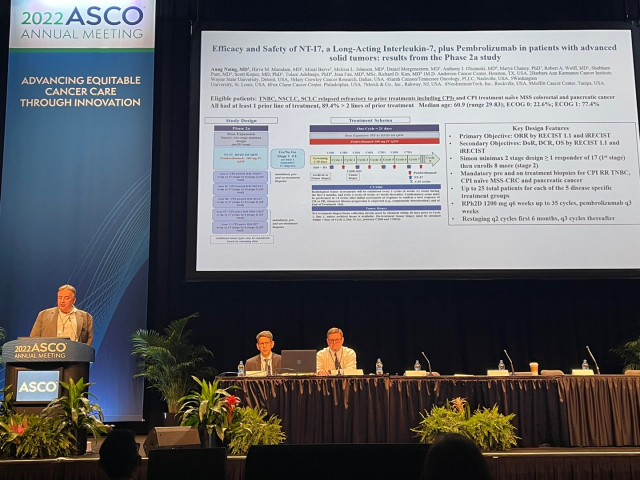
네오이뮨텍(950220)은 T세포 증폭 유도 신약 물질 ‘NT-I7’과 면역관문억제제, 키메릭항원수용체 T세포(CAR-T) 병용 임상 등 총 3건의 포스터를 공개하고 유의미한 임상 시험 결과 데이터를 발표했다. 양세환 네오이뮨텍 대표는 “면역관문억제제와 NT-I7의 병용 임상에서 국소진행성(MSS) 대장암과 췌장암이 우선 개발될 가능성을 보인데 이어 고형암 전반에서 안전성과 함께 질병통제율이 나타나기 시작했다"며 “현재 진행중인 임상의 최종 데이터가 확인되면 구체적인 허가 임상 디자인을 도출할 예정”이라고 설명했다.
이외에도 에이비온(203400)은 고형암 항암제 ‘ABN401의 임상1상을 통해 안전성과 유효성을 확인하고 2상에 대한 적정 용량을 확인했다고 발표했다. ABN401은 간세포성장인자수용체(c-MET)를 표적으로 하는 고형암 치료제다. 회사 관계자는 “글로벌 제약사를 대상으로 기술 수출에 나설 계획”이라고 말했다. 엔지켐생명과학(183490)은 화학·방사선요법 유발 구강점막염(CRIOM) 신약 후보물질인 ‘EC-18’ 기술수출 논의를 구체화할 예정이다. 회사 관계자는 “질의응답 과정에서 전문가들이 임상 3상 연구에 대해 큰 기대감을 표시했다”며 “라이선싱 아웃 협상 결과에 따라 글로벌 제약사와 공동으로 임상 3상 계획서를 만들어 FDA에 낼 예정”이라고 말했다.
이밖에 의료 인공지능(AI) 기업 루닛은 AI 바이오마커 '루닛 스코프'의 암 치료 활용 가능성을 입증한 연구 결과 등 11개의 연구초록을 발표해 주목을 받았다. 메드팩토는 췌장암 대상 ‘백토서팁+폴폭스' 병용 요법 임상 중간 데이터를 온라인 공개했다.