면역항암제 개발 기업 유틸렉스가 임상 단계 파이프라인의 미국 진출 기대감에 힘입어 개장 직후 상한가로 직행했다.
28일 오전 11시 현재 유틸렉스는 전거래일(27일) 대비 가격제한폭(29.9%)까지 오른 7740원에 거래 중이다. 거래량은 600만주에 육박하며 평소보다 5~6배 이상 뛰었다. 초기 임상단계인 '앱비앤티셀(EBViNT)'이 미국식품의약국(FDA)으로부터 희귀의약품 지정(ODD)을 받았다는 소식에 매수세가 몰린 것으로 풀이된다.
이날 유틸렉스는 킬러T세포치료제 ‘앱티앤티셀(개발코드 EU204)’이 FDA로부터 희귀의약품 지정을 받았다고 공시했다. 앞서 지난 7월 EU204의 희귀의약품 지정 신청을 했다고 밝힌지 2개월 여만에 승인 결과를 공개한 것이다.
유틸렉스는 올해 초에도 앱티앤티셀을 투여받은 NK/T세포림프종 환자가 완전관해에 도달했다고 밝히며 상한가를 기록한 바 있다.
희귀의약품 지정은 환자 수가 20만 명 이하로 치료제가 없는 희귀난치성 질환에 대해 치료제 개발 및 허가가 신속하게 이뤄지도록 지원하는 제도다. FDA 희귀의약품으로 지정되면 신속심사, 임상 보조금 지원, 임상 2상 이후 조건부 판매 등의 혜택이 제공된다.
유틸렉스는 미국 샌디에이고 소재의 현지 법인 유틸로직스를 설립하고 '앱비앤티셀'을 비롯해 핵심 파이프라인의 임상을 한국과 미국 투트랙으로 진행하기 위한 전략을 구사하고 있다.
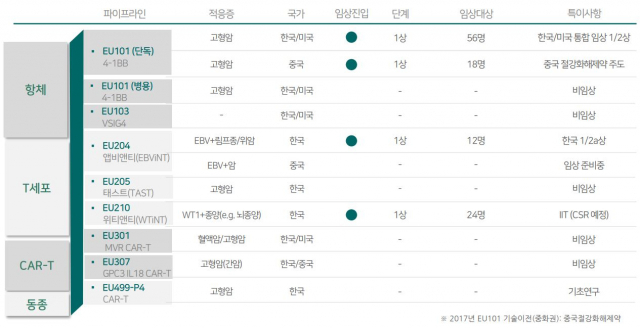
앱티앤티셀은 현재 앱스타인바바이러스(EBV) 양성 림프종 및 고형암(위암) 환자를 대상으로 국내 임상 1/2a상을 진행 중이다. 회사 측에 따르면 별도로 진행 중인 연구자임상(IIT)을 포함해 현재까지 총 3명의 NK/T세포림프종 환자에게 앱티앤티셀 투여가 이뤄졌다. 그 결과 3명 모두 암세포가 완전히 사라진 완전관해에 도달한 것으로 확인한 바 있다.
앱티앤티셀은 환자로부터 추출한 T세포 가운데 표적하는 암에 반응하는 T세포만을 모아 배양한 뒤 다시 투여하는 기전의 킬러T세포 치료제다. 복잡한 유전자조작을 거치지 않아도 된다는 점에서 카티세포치료제보다 제작이 단순하지만, 환자당 1대1 맞춤형으로 제작해 투여한다는 점은 유사하다.
2018년 12월 코스닥시장에 상장한 유틸렉스는 자체 플랫폼 기술을 토대로 항체 기반의 다양한 세포치료제를 개발 중이다. 코로나19 유행 이후에는 진단제품 및 치료제, 백신 개발 등을 추진하면서 주가가 고공행진했다. 코로나19 유행이 한창이던 작년 9월에는 주가가 2만5000원 대까지 치솟으면서 시가총액이 4000억 원을 넘겼지만, 확산세가 사그라들면서 주가가 줄곧 내리막을 걸었다.
◇Why 바이오는=‘Why 바이오’ 코너는 증시에서 주목받는 바이오 기업들의 이슈를 전달하는 연재물입니다. 주가나 거래량 등에서 특징을 보인 제약·바이오 기업에 대해 시장이 주목한 이유를 살펴보고, 해당 이슈에 대해 해설하고 전망합니다. 특히 해당 기업 측 의견도 충실히 반영해 중심잡힌 정보를 투자자와 제약·바이오 산업 관계자들에게 전달합니다.